- 1Opencv怎么使用呢?opencv使用完整教程分享_opencv怎么用
- 2YOLOv5源码逐行超详细注释与解读(7)——网络结构(2)common.py_yolov7缺少common.py
- 3Python环境下一种基于改进小波变换的信号时频分析方法
- 4Linux命令之 systemctl 指令_liunx systemctl 命令
- 5Unity之UGUI的学习(一):Canvas和EventSystem(画布和事件系统)_unity canvas event
- 6Docker中部署flink集群的两种方式
- 7Flutter和Rust如何优雅的交互_flutter rust
- 8高级语言期末2011级A卷(软件学院)
- 9PostgreSQL 15版本新特性一览_postgresql15
- 10ConnectionRefusedError: [Errno 111] Connection refused问题解决_kombu.exceptions.operationalerror: [errno 111] con
EEG微状态的皮层电图激活模式_seeg动态脑网络分析
赞
踩
前言
脑电图(EEG)微状态是表征大脑静息态网络自发激活的短暂连续的稳定头皮场电位。脑电微状态被假定介导局部活动模式。为了验证这一假设,本研究将瞬时全局脑电微状态动力学与皮层脑电图(ECoG)和立体定向脑电图(SEEG)深度电极记录的局部时间谱演变相关联。假设这些相关性与伽马波段有关,并且这些相关性的解剖位置与先前使用fMRI-EEG或EEG源定位的研究一致。本研究分析了两名参与者同时进行无创头皮EEG和有创ECoG和SEEG记录的静息态数据(5分钟)。采用硬膜下和颅内电极对耐药性癫痫患者进行术前评估时记录数据。经过标准化预处理后,将一组标准的微状态模板图拟合到头皮EEG数据中。利用EEG微状态时间线的协方差映射和ECoG/SEEG的时间谱演变作为输入,发现了特定微状态类别在不同频段(θ、α、β和高频γ)中ECoG/SEEG局部场电位激活的系统性变化。本研究发现,在所有四个频段中,ECoG/SEEG频谱振幅与微状态时间线存在显著的共变(p=0.001,置换检验)。两名参与者在不同微状态下的ECoG/SEEG电极的协方差模式相似。据所知,本研究是第一项证明与同步EEG微状态相关的频域ECoG局部场电位激活/失活模式的研究。
前言
包括脑电图(EEG)、功能性磁共振成像(fMRI)和脑磁图(MEG)在内的独立研究提出这样的假设:静息态大脑活动是一个主动的自组织过程,即使在没有传入刺激的情况下也是如此。在脑电研究中,微状态分析已成为可以量化静息态网络活动的可靠工具。由于微状态是一种准稳定、大规模头皮场电位的短连续周期,因此它们代表了大脑静息态网络的自发激活。与静息态fMRI网络类似,在过去的二十年里,人们发现了一组相对较小且可复制的原型脑电微状态类别;然而,区分状态的数量通常比fMRI研究报告的要少。
人们假设,脑电微状态代表了相对缓慢和高度同步振荡的单一和全局模式,这些振荡调节活动并控制局部大脑结构之间的相互作用,以动态地调整大脑对瞬时环境和内部条件的反应。精神分裂症和痴呆等功能障碍性精神状态在特定类别的脑电微状态中有典型的变化。这种适应性调节机制被认为是基于皮层兴奋性的瞬时低频波动,这些波动是全局组织的(连贯性交流 [CTC]),并调节主要发生在高频(高伽马)范围内的局部大脑结构之间的活动和相互作用。因此,(在当前理解的假设下)脑电微状态和局部高频活动系统地相互作用,但存在不同的现象;微状态被认为是关于整体认知模式的信息,而局部活动被认为包含特定的表征内容。然而,脑电微状态与高伽马皮层振荡的局部变化之间的直接联系尚未建立。使用EEG-fMRI对脑电微状态相关的局部大脑活动进行的研究表明,与特定的全局微状态模式相关的局部激活变化模式是一致的。然而,由于fMRI的时间分辨率较低,它们在频率效应方面缺乏表征。同样,使用脑电逆解的研究确定了脑电微状态的收敛定位。然而,他们没有解决与这些微状态相关的假定局部活动变化可以通过解析频域数据来区分的问题。这种限制也可归因于这样一个事实,即头皮EEG中皮层活动的更多焦点模式被抑制,因为EEG导联场起到了空间低通滤波器的作用。
本研究通过将头皮脑电微状态分析与皮层脑电图(ECoG)和立体定向脑电图(SEEG)相结合来解决这一问题,这两种脑电图旨在专门捕捉局部大脑活动。颅内局部场电位的记录提供了良好的空间和时间分辨率。此外,ECoG和SEEG记录具有相当大的风险,但它们可以在一定程度上改善局部宽带高伽马活动的测量,从而证明其在癫痫等临床条件下的应用是合理的。特别是,宽带高伽马可以提供出色的空间分辨力。此外,宽带高伽马被认为是皮层加工的一般指标。因此,本研究假设宽带高伽马活动的瞬态和局部变化始终与特定EEG微状态类别的存在与否有关。
基于CTC理论,本研究提出了以下两个假设:(1)基于头皮EEG的全局微状态模式与颅内局部场电位激活模式相关,并且这种相关性与频率有关;以及(2)这些相关性的解剖位置与先前使用fMRI-EEG联合或EEG源定位的研究一致。
材料和方法
参与者
数据来自两名成年参与者,使用硬膜下和立体定向深度电极对耐药性癫痫进行了术前评估。电极的放置完全由临床考虑决定,两名参与者都提供了参与研究的书面知情同意书。图1总结了患者信息、电极覆盖范围和特定癫痫诊断。参与者以德语为母语,右利手,语言优势半球为左半球。这项研究在弗赖堡大学诊所(Freiburg,Germany)进行,并得到了德国弗赖斯堡大学伦理委员会的批准。

图1.两名参与者的MRI结果和电极位置。
EEG、ECoG和SEEG记录和数据简化
数据是在德国弗赖堡大学医学中心的癫痫中心收集的。通过硬膜下网格电极、条状电极以及根据医疗需要放置的深度电极记录EEG信号。使用Neurofile NT数字化视频EEG系统(Natus Medical Inc.,San Carlos,CA,USA)以1024Hz的频率采集EEG、ECoG和SEEG数据。本研究使用了5分钟的静息态记录。
电极定位
对于两名参与者,使用分辨率为1×1×1mm的共配准和归一化术前和术后磁共振成像(MRI)以及Stolk等人(2018)的自动可视化方法来确定电极位置,该方法是FieldTrip工具箱的一部分。简要总结如下:将植入前的MRI结果转换到Talairach空间。然后,使用FreeSurfer 5.3.0对MRI结果进行分割。使用Kovalev等人(2005)描述的自动可视化方法确定三维电极坐标。将电极配准到蒙特利尔神经研究所(MNI)空间的模板大脑上,以便于可视化。MNI重建仅用于可视化目的,但电极定位是在个体空间中确定的。图1提供了参与者的ECoG和SEEG电极位置的概述。头皮EEG电极根据传统的10-20系统放置。
发作间期癫痫放电检测
在进行所有微状态分析之前,首先使用已建立的自动算法检测所有通道的发作间期癫痫放电(IED)。将连续EEG/ECoG/SEEG信号进行25~80Hz的滤波(二阶有限脉冲响应),并使用MATLAB中的希尔伯特(Hilbert)变换提取解析幅值,并进一步确定数据的z分数。IED事件被定义为在20ms~100ms期间高于均值三个标准差的信号。事件前后2.5s的周期包含了伪影周期。
预处理
使用Brain Vision Analyzer 2.2对EEG、ECoG和SEEG数据进行分析。采用独立成分分析校正EEG通道中的眼动伪迹。对伪迹过多的EEG通道进行插值。对ECoG网格电极进行50Hz的陷波滤波,并应用网格内共同平均参考。ECoG条状电极和SEEG参考其直接侧邻电极(双极蒙太奇),并降采样至500Hz。对头皮EEG数据进行2~20Hz的带通滤波,并重新计算为共同平均参考值。
微状态分析
本研究计算了每个样本随时间的变化,参与者EEG的全局场功率(GFP)量化了一组电极的总体电位变化。然后,将GFP峰值处的地形图分配给Custo等人(2017)报告的七个微状态模板中的最佳拟合模板。为此,使用球面样条插值将这些模板在空间上重采样到10-20系统。之所以选择这些模板图,是因为它们基于大型标准样本,并且它们的逆解已经发表。基于瞬时GFP峰值矩的分配,使用最近邻插值方法对剩余数据进行插值。这为每个微状态类别生成了一个时间线,该时间线指示了由给定微状态类别的微状态模型可以解释的EEG方差量(当数据未分配给给定类别时为零)。然后,将这些时间线作为SEEG和ECoG数据的回归量进行协方差分析。
协方差映射
为了估计不同频段中ECoG和SEEG局部场电位的瞬态激活/失活,本研究计算了其时空演变过程:首先,使用IIR带通滤波器,对数据进行不同频带(θ:4-8Hz;α:9-12Hz;β:13-30Hz;低伽马:30-70Hz;宽带高伽马:70-150Hz)的带通滤波。然后,对数据进行整流,在给定频段的低截止频率的一半截止值处进行低通滤波,并进行对数变换。
对于每个ECoG和SEEG通道,时间谱演变与给定微状态类时间线的协方差被计算为该微状态类时间线在同一时刻的加权平均值。剔除有伪影的时间段。对每个参与者进行这种协方差分析,得出每个参与者在每个频段的beta值(协方差图)以及ECoG和SEEG数据的微状态类的单独分布。使用1000次迭代的置换检验来检验这些协方差图的显著性。为了估计所获得的协方差图与微状态时间线的关联强度,将得到的协方差图反向投影到ECoG/SEEG数据的相应时间谱演变上,从而得到每个协方差图的单个时间进程。然后,将这些时间进程与相应的微状态时间线进行相关分析,以估计R值。这里只给出了R值大于0.1的结果(图2)。

图2.左外侧图显示了Custo等人(2017)的七个微状态模板地形图。将这些微状态模板图拟合到每个时间段的静息态头皮EEG数据上,得到了7个时间线来表示不同微状态类的存在和强度随时间的变化(左下图)。使用网格和深度电极记录ECoG和SEEG的结果如中上图所示,并首先在各自频段(蓝线)、校正(红线)和低通滤波(黑线),从而得到每个颅内通道的时间谱演变。最后,以微状态时间序列为权值,通过计算这些时间谱演变的加权和得到协方差图。在参与者1的微状态C类中,α频段的协方差图如右图所示。
聚类分析
为了测试两名参与者的微状态图与Custo等人(2017)的微状态模板的对应程度,本研究将标准极性不变的k-均值聚类(其中k设置为7)应用于每个参与者的全局场功率瞬时峰值处的地形图上,并计算得到的单个微状态图和模板的相关系数。
结果
本研究通过应用Custo等人的七个模板来估计随时间变化的头皮EEG微状态模式。然后,以这些头皮EEG微状态的时间动态以及ECoG和SEEG活动的时空演变作为输入,进行协方差分析。研究结果发现,对于使用ECoG电极的两名参与者,在所有频段的所有七个微状态类别上均有显著的协方差图(p<0.0001,置换检验)(图3A)。此外,本研究还发现参与者1的微状态C类和参与者2的微状态D类的相关系数最高。

图3.(A)使用ECoG电极获得的R值作为两名参与者微状态类别和频段的函数。参与者1的微状态类别C和参与者2的微状态类别D的相关性最高。(B)参与者1和2的大脑左右半球的协方差图。
相应的ECoG电极处的协方差图值确定了与特定微状态类别存在相关的正和负β值的不同解剖区域。其中,微状态C类的β值最大,位于参与者1的左赫氏回和颞上回。左颞内侧回和颞下回的β值较小。此外,本研究发现在较高频率(β、低γ和高γ)下,右颞下回的β值较大。低频段(θ,α)和高伽马频段的激活模式相反,表明低频段中的负β值与高伽马频段中的正β值相关(图3B上图)。
与微状态D类相关的β值在参与者2的缘上回、躯体感觉回下部和额回下部最大。此外,本研究发现楔前叶中线处的β值较大(图3B)。在参与者2中,低频(θ和α)的β值与宽带高伽马之间存在同样的反比关系(图3B下图)。
一般来说,低频段(θ,α)和高伽马频率之间的反比关系在所有微状态中都很普遍。关于覆盖海马体和杏仁核的SEEG电极,本研究在所有频段和微状态类别上都观察到了显著的结果;但R值仅在微状态D类中比较大(>0.1)。
最后,将两个参与者的协方差图分解为感兴趣的目标区域。使用BioImage Suite识别不同感兴趣区域的电极。图4显示了这些感兴趣区域的所有微状态类别的θ和宽带高伽马活动的平均β值。此外,本研究再次观察到与微状态D类相关的θ和高伽马之间存在反比关系。
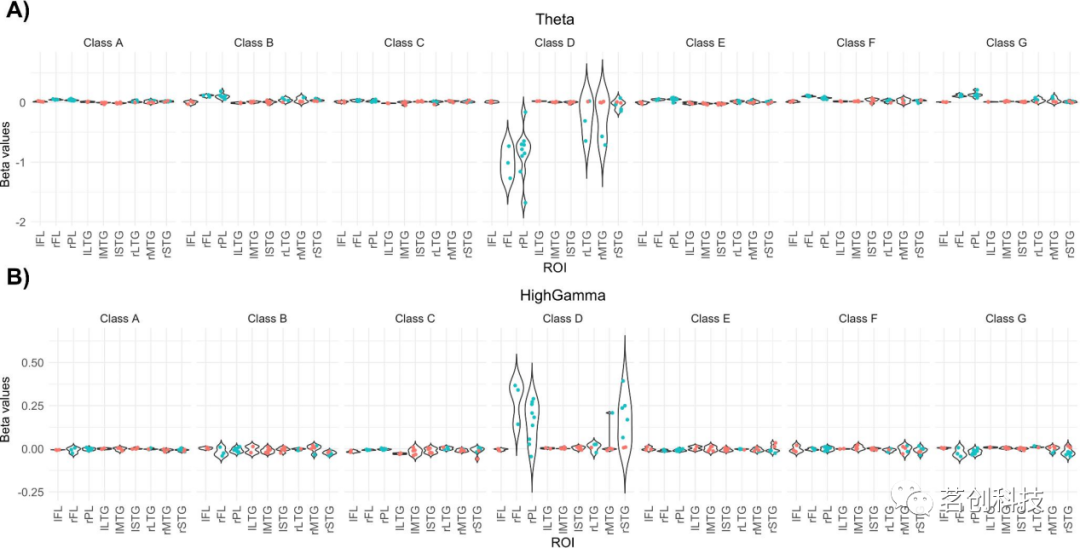
图4.两名参与者(参与者1:红色;参与者2:蓝色)的θ(上图)和宽带高伽马(下图)频段关键解剖区域的平均β值。
此外,本研究对头皮EEG结果进行了聚类分析(见补充材料8)。这些图谱与Custo等人的模板图谱非常相似,平均相关系数r=0.80(参与者1)和r=0.86(参与者2)。
讨论
本研究证明了基于全局头皮EEG的微状态动力学与颅内活动的局部频域变化(包括宽带伽马活动)系统相关。通过将头皮EEG微状态分析与ECoG/SEEG局部场电位数据的时间谱演变相结合,本研究提出了一种新的方法,该方法可以潜在地减少先前研究EEG-fMRI和基于逆解的EEG研究的技术限制。为了将基于头皮EEG的微状态动力学与ECoG/SEEG信号相关联,本研究使用微状态激活时间线作为ECoG/EEG局部场电位的时间谱演变的回归量。因此,我们能够以毫秒级的分辨率捕捉微状态类别的快速变化,并将本研究的分析扩展到宽带高伽马频段,该频段反映了具有高空间分辨率的局部神经元群的活动。
本研究的方法使我们能够以相同的时间分辨率将直接从皮层电极获得的局部场电位数据与基于头皮EEG的微状态相关联。因此,该方法有可能进一步解开局部激活/失活与全局微状态之间的相互作用。为今后探索基于ECoG的连接和基于EEG的微状态研究提供了基础。
此外,本研究成功地证明了频域ECoG和SEEG局部场电位的不同激活模式与同时存在特定类别的全局头皮EEG微状态有关。这些关联取决于频段和ECoG的位置。这种复杂的皮层激活和失活模式与最近的脑电微状态研究的观点一致。首次探讨脑电微状态的BOLD相关性的研究结果发现,这些微状态与BOLD信号的增加和减少均有关。微状态依赖的激活/失活模式取决于频段,宽带高伽马活动与低频段活动呈反比关系。这一点特别重要,因为人们认为微状态介导局部瞬态神经活动,而这种活动不需要足够长的时间来建立网络水平的协调。因此,宽带高伽马活动可能反映了由头皮微状态模式调节的短时间区域激活。
本研究对宽带高伽马和低频谱之间负相关的发现也与其他研究一致。然而,正如CTC框架所假设的那样,ECoG/SEEG电极的微状态动力学与低频段(例如α)之间的相关性可能反映了长程功能连接的调节。总之,本研究提供的初步证据表明,全局头皮EEG微状态与ECoG/SEEG场电位相关。这些相关性在低频和高频段之间存在系统性的反比关系。这些结果强调了复杂自组织的概念,即使在没有具体外部刺激的情况下也是如此。
原文:Mikutta, C.A., Knight, R.T., Sammler, D. et al. Electrocorticographic Activation Patterns of Electroencephalographic Microstates. Brain Topogr (2023). https://doi.org/10.1007/s10548-023-00952-1


