- 1比较完整的NAT(网络地址转换)配置_nat转换配置详解
- 2TensorFlow框架用Python搭建神经网络八股:准备,前传,后传,迭代_神经网络设计八股准备, 前传, 反传, 迭代进行总体设计.
- 3Linux (九)服务器环境搭建_linux环境搭建 小帅
- 4基于Python爬虫湖南长沙天气预报数据可视化系统设计与实现(Django框架) 研究背景与意义、国内外研究现状
- 5Python练习篇15-with语句介绍_使用with语句打开文件“text1.txt”
- 6qt5 windows Excel QAxObject导入导出_qt多表格输出qaxobject
- 7挑战30天学完Python:Day21 类和对象
- 8IDEA运行selenium程序提示错误:Exception in thread “main“ org.openqa.selenium.SessionNotCreatedException:_command: [null, newsession {capabilities=[capabili
- 9UNIX环境编程学习笔记(27)——多线程编程(二):控制线程属性
- 10Datawhale 李宏毅机器学习笔记_李宏毅交叉验证
阿尔茨海默病临床试验中静息脑电节律的测量_静息态脑电采集
赞
踩
电生理专业兴趣领域(EPIA)和全球大脑协会对阿尔茨海默病(AD)临床试验中候选脑电图(EEG)测量方法的推荐得到了认可。专家组审查了该领域的文献。最一致的发现是,轻度认知障碍和痴呆的AD患者在疾病进展和干预过程中,后部alpha(8-12 Hz)和广泛的delta(< 4 Hz)以及theta(4-8 Hz)节律的峰值频率、功率和“相互关联性”出现异常。达成以下共识:(1)需要对患者的指导、静息态EEG(rsEEG)记录方法以及选择无伪迹的rsEEG时段进行标准化;(2)在delta、theta和alpha频段,可以使用功率密度和“相互关联性”rsEEG测量方法(例如,定向传递函数、相位滞后指数、线性滞后连通性等)进行AD患者的分层以及对疾病进展和干预的监控;(3)为了达到监管目的,国际多部门的合作是必要的。本文发表在Alzheimer’s & Dementia杂志。
本文亮点:
静息状态电脑脑图(rsEEG)测量可能反映人类皮层神经元的同步性。 阿尔茨海默病(AD)患者在群体和个体水平上都表现出rsEEG测量的一致性异常。 线性EEG测量可能被用作AD临床试验中的神经生理标记。
研究背景:
系统回顾:阿尔茨海默病协会国际推进阿尔茨海默病研究和治疗社会(ISTAART)电生理专业兴趣领域和全球大脑联盟的现有小组回顾了相关领域的文献,并就与阿尔茨海默病(AD)中的临床表型和神经影像标志物一致相关的静息状态电脑脑图(EEG)测量达成共识。
解读:轻度认知障碍和痴呆的AD患者在疾病进展、神经影像标志物和干预措施的关系中,后部alpha(8-12 Hz)和广泛的delta(< 4 Hz)以及theta(4-8 Hz)节律的峰值频率、功率和“相互关系”中均显示出一致的异常。我们提出“生理生物标志物”(P+或P-)这个术语,用于描述这些EEG测量,可能反映出AD相关的皮质下和丘脑皮质环路以及上行激活系统的脆弱性,这些信息对精准医学了解AD的状态和进展具有丰富的价值。
未来方向:国际计划将使用并交叉验证这些EEG测量,以便在AD临床试验中系统地使用。
合格的生物标记物用于临床试验中阿尔茨海默病患者的诊断和监测
国际工作组(IWG)和美国老年病研究所-阿尔茨海默病协会研究框架(NIA-AA Research Framework)最近提出并完善了关于临床试验中阿尔茨海默病(AD)在无症状前期,早期(具有轻度认知障碍的AD,即ADMCI)和明显痴呆(ADD)阶段的诊断和监测的建议和研究标准,这些都是基于活体液体和神经影像生物标记物。根据这些诊断标准,AD状态与以下因素相关:(1)脑脊液(CSF)中的淀粉样β(Aβ)减少和大脑级别的淀粉样物质增加,这可以通过淀粉样PET映射揭示,和(2)CSF中的磷酸tau增加和tau PET示踪剂保留增加。随着疾病进程的发展,神经退化可能通过18氟脱氧葡萄糖PET(FDG-PET),CSF中的总tau,以及颞顶皮质和中央颞叶(包括海马)的大脑萎缩的磁共振成像(MRI)来揭示。
闭眼休息状态电脑脑波节律的测量
以上的神经影像技术用于纵向AD临床试验的连续记录可能受到其高成本和侵入性的限制,特别是在低收入和中等收入国家。除了FDG-PET作为突触完整性标记的间接作用外,这些生物标记物都没有反映AD神经病理学对大脑神经信号传输的影响,这是支撑认知过程的神经生理学。这是在阿尔茨海默病研究中的生物标记物的淀粉样病变,tau病变,和神经退化框架中的“生理学空白”。
为了填补这个空白,闭眼休息状态电脑脑波(rsEEG)节律的测量非常有希望,因为它们是非侵入性的,可重复的,具有成本效益,且基于在全球范围内广泛可用的记录技术,包括在低收入和中等收入国家。这些测量可能探查AD对上行激活系统和互惠的丘脑皮层回路的影响,其中振荡的(去)同步信号动态地支撑皮层唤醒。 这种皮层神经活动的相位同步/解同步可能以相互关联的方式发生在多个皮层区域,控制局部和长距离神经网络内的动作电位的传输和通信。动物研究阐明了持续EEG活动在皮层和皮层下级别的细胞和分子基础。此外,它们表明AD神经病理学可能导致神经细胞之间的断连,皮层-皮层和皮层-皮层下通路的损害,以及可能与皮层神经过度兴奋和过度同步以及减少的神经传输,神经信号和突触活动相关的髓鞘轴突的损失。
在临床环境中,通常从19-25到> 80的头皮电极记录rsEEG活动,这些电极按照10-10电极系统(Seeck等人。;图1)放置,而病人在闭眼静息的清醒状态下。他们被指示保持心理-生理放松,无认知需求,并允许他们的思绪自由漫游(框1)。

图 1:临床电脑脑波(EEG)记录的10-10头皮电极贴片系统的改良组合命名法,扩展了下链的前后电极。
由于头骨和头皮的阻抗特性,在头皮级别记录的rsEEG节律主要由频率表示,大约从1到100 Hz,通过EEG记录系统的高时间分辨率(<1 ms)可以检测到。
与上述神经影像技术相比,EEG技术的空间分辨率较低到适中(即,几厘米)。的确,在头皮电极测量的rsEEG活动可能源自位于几厘米远的皮质源或分布在大区域,这是由于头部容积传导效应(> 10 cm2; 20)。这个分辨率取决于头皮EEG电极的数量和用于EEG源估计的数学技术(图2)。

图2 测量方法的空间和时间分辨率尺度的示意概览,用于电生理学和功能性神经影像学。
测量方法包括电脑脑图(EEG)、磁脑图(MEG)、近红外光谱(NIRS)、功能性磁共振成像(fMRI)、电皮层图(ECOG)、局部场电位(LFP)记录、微电极阵列(MEA)记录和微电极(ME)记录。非侵入性方法以蓝色显示,侵入性方法以红色显示。
在无干扰的rsEEG活动中,后部(“主导”)的α节律(≈8-12 Hz)是主导的振荡,并在从闭眼到睁眼的转换中幅度减小,这是由于视觉-空间皮层系统的激活。 在安静的警觉状态(无任务要求)下,低频α节律(≈8-10 Hz)的高幅度可能反映了大脑唤醒、注意力和准备度的低水平,而高频α(≈10-13 Hz)和低频β(≈12-20 Hz)节律的高幅度可能反映了感知、体感运动和记忆过程的低水平。
在感觉运动和认知事件期间,α节律被更快的皮层rsEEG振荡所取代,即高频β(20-30 Hz)和γ(30-70 Hz)节律,主要由(1)前脑胆碱能直接输入到海马体和大脑皮层以及(2)丘脑皮层投影所驱动。
在健康的成年人中,rsEEG活动在δ(1-4 Hz)和θ(4-7 Hz)节律处可能通常显示出小幅度,并在感觉运动和认知事件期间展示出复杂的变化模式。 因此,在休息状态条件下θ或δ节律异常突出被认为是大脑功能障碍的迹象。
多种方法可以探测无伪迹的头皮rsEEG波形中嵌入的信息(详见支持信息中关于用于阿尔茨海默病研究的静息状态EEG测量的主要特征)。快速傅里叶变换(FFT)假设rsEEG信号是线性的,并返回每个头皮电极上rsEEG电压时间序列的“局部”功率密度,逐个频率区间进行计算(图3)。其他方法根据rsEEG信号的线性或非线性假设,估计头皮电极对或EEG源之间的“rsEEG活动的相互关系”,而图论指数则表示这些估计的整体拓扑特征,即由边连接(或不连接)的网络节点(Box 2)

图3 电脑脑图(EEG)节律分解为EEG功率谱的示意图。
草图举例说明了在δ、α和β节律的频率区间的正弦EEG波形,以及它们如何被表示(1)当在给定的相位处互相求和或(2)作为计算EEG功率密度谱的输入。
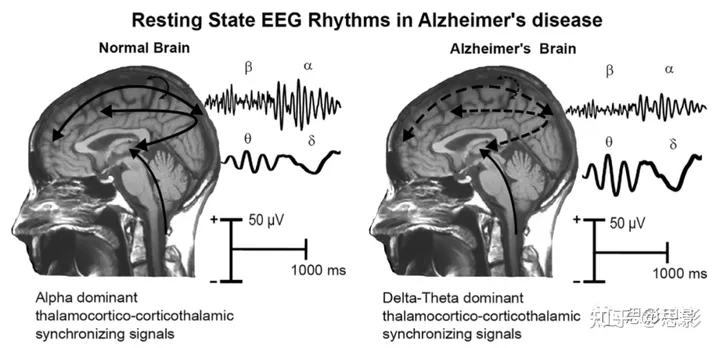
图4 年龄匹配的老年认知无损(CU)人群和阿尔茨海默病(AD)患者大脑中静息状态闭眼脑电图(rsEEG)节律生成的初步生理模型。
在正常脑部,主导的脑电图节律在阿尔法频率(8-12 Hz)上观察到,这表示大约10 Hz的神经网络自发同步,调节主体的全局唤醒和意识状态的波动。这些网络涵盖了大脑皮层、丘脑、基底前脑和脑干的神经元群,包括谷氨酸能、乙酰胆碱能、多巴胺能和5-羟色胺能的网状升支系统。在AD患者的脑部,这些节律的振幅减小(即持续背景去同步),同时病理性的rsEEG慢频率(包括δ波<4 Hz和θ波4-7 Hz)的振幅增加。这种rsEEG节律的“减慢”主要反映了一种丘脑皮质“失连接模式”。
将rsEEG测量包括在阿尔茨海默病(AD)临床试验中(例如,患者的分层、监测疾病进展、治疗效果等)作为丰富的神经生理生物标志物,必须基于一个初步的证明,即这些测量是可靠的、一致的和敏感的(例如,重测可靠性,效应和样本大小等)。例如,给定rsEEG测量的统计功率和效应-样本大小的可变性是评估该候选生物标志物是否可以包括在针对AD患者设计的> 1阶段的临床试验协议中的相关参数,即测试新药对AD的神经生物学效果和治疗效果的协议。应考虑到,2期和3期的临床试验通常分别涉及每个患者群体的100到300名和300到3000名患者。 因此,适合的rsEEG生物标志物预期是可靠的、一致的,并且每组的样本大小明显低于n = 300名患者。
关于测试-重测可靠性的问题,以往的研究报告显示,在健康成年人进行的12至40个月的重测中,无人工干扰的rsEEG节律的功率密度是稳定的。具体来说,这些研究显示了高的测试-重测相关性(r = 0.92,5分钟,r = 0.84,12-14周;类内相关系数 = 0.8-0.9,4周)。此外,当从持续20、40、60秒至4分钟的无人工干扰的rsEEG数据中计算出来时,包括闭眼状态下的主导后部alpha节律在内的rsEEG活动的绝对和相对功率密度都相当一致,这些都是在临床神经生理学中用于定量分析的典型的rsEEG数据集的持续时间。
总的来说,以往的测试-重测研究的结果显示,rsEEG相对功率密度的可重复性略高于绝对功率密度,这可能是因为标准化程序有减少测量变异性的一般属性(例如,段等人)。此外,眼睛闭合状态下的频谱rsEEG测量的再现性高于眼睛睁开状态,这可能是由于用于rsEEG频谱分析的数据中的残留眨眼和扫视的影响。此外,rsEEG测量的可再现性在rsEEG功率密度中高于在传感器和源级别的相互关联性(连通性)估计。最后,这种可再现性在传感器级别略高于源级别,但这些发现鼓励在临床应用中使用两种分析级别。
Box 1:人类静息警觉(静息状态)下电脑脑电图(EEG)活动记录的实验条件
神经生理机制,持续时间,及指示
保持低警觉状态并闭眼数分钟(即5-15分钟或更长时间)的神经生理机制。它也探测了昏昏欲睡和睡眠的过渡,因此在出现睡眠时,实验者(或训练有素的技术人员)不应提醒受试者。指示受试者安静地坐着,保持放松的心态,让思绪自由飘扬(即没有以目标为导向的心理活动),并闭上眼睛。 在连续开闭眼时,调节警觉水平增加和减少的神经生理机制(即5-10分钟)。在实验者的提示下,眼睛的开闭时间很短(即1分钟),眼睛的开闭顺序会重复(即两到四次)。对受试者的指示与第一种条件相同。在出现睡眠的情况下,实验者需要提醒受试者,以得到足够与适当心理状态相关的EEG数据。第三种条件测试了在闭眼(即3-5分钟)时保持低警觉状态和在睁眼(即3-5分钟)时保持中等警觉状态的神经生理机制。对受试者的指示与第二种条件相同。
Box 2:图论建模rsEEG相互关联活动的度量拓扑
在rsEEG研究中的Gore图指数:
“聚类系数”是图中节点倾向于聚集在一起的程度。 “路径长度”是任何节点需要到达图的其他部分的边的平均数量。 “介数中心性”是一个节点需要达到图的所有其他节点的边的数量(数字越小,中心性越高)。 “聚类系数”是图中节点倾向于聚集在一起的程度。 “局部效率”是在节点邻域上计算的,与聚类系数(“全局效率”)有关,作为网络节点之间有效交换信息的度量。 “模块性”是网络可以被划分为明确定义的组的程度。 “小世界性”被定义为强烈的本地连接性和有效的“中心”连接远节点之间的良好平衡。 “鲁棒性和适应性”是一个网络在一部分节点(链接)受损时保持其连接性的能力。
考虑到以上数据和考虑因素,健康成人衍生的典型rsEEG测量的可靠性和一致性似乎总体上适合于临床神经生理学的应用。然而,这些统计特性应当被仔细考虑,以解释使用rsEEG测量来比较AD和对照个体,以及研究AD进展和疗法反应的研究中报告的统计效应。
目标和方法
尽管国际专家小组已经强调了rsEEG测量在AD研究中的优点,但是仍然对不同rsEEG测量在AD临床试验中的具体生物标记物价值(如疾病状态,进程等)存在不确定性,可能是因为可用的方法论方法的异质性。为了澄清这些不确定性,阿尔茨海默病协会和全球大脑联盟的电生理专业兴趣区域(EPIA)支持由一个多学科专家小组撰写的这篇文章,以提供关于AD临床试验的候选rsEEG测量的建议。核心问题是“是否有rsEEG测量能在以往在AD患者中进行的研究中显示出一致的效应,以便在未来的临床试验中用于患者的分层、疾病进程的监测以及干预效果的研究?”小组的专业知识涵盖了与核心问题密切相关的多个相关学科(如神经学、精神病学、痴呆症的神经成像;临床神经生理学;痴呆症rsEEG节律的定量分析;认知神经科学;公共卫生)。
专家小组根据通过Web of Science、Scopus和MEDLINE进行的领域文献的全面审查,使用以下关键词的几个适当组合,制定了建议。
对于“关心的人群”,使用了以下关键词:“主观记忆抱怨”(SMC),“主观认知抱怨”(SCC),“轻度认知损害”(MCI),“轻度神经认知障碍”,“阿尔茨海默病病理”,“阿尔茨海默病”(AD),“阿尔茨海默病病症状”(DAT),“重大认知损害”,“重大神经认知障碍”和“痴呆”。
对于“关心的EEG技术”,使用了以下关键词:“电脑脑电图(EEG)”、“静息状态EEG”、“持续EEG”、“背景EEG”、“定量EEG(qEEG)”、“脑节律”和“脑震荡”。
对于“关心的EEG测量”,我们使用了以下关键词:“波形(即对在持续rsEEG痕迹上观察到的众所周知的图形元素的视觉分析和描述),“EEG功率密度”,“相对功率密度”,“alpha峰频率”,“复杂性和不规则性(指一个头皮电极的时间模式的动态或许多头皮电极的时空模式)”,“EEG活动的相关性或EEG源连接性”,“频谱相干性”,“部分相干性”,“熵”,“混沌”,“信息理论”,“格兰杰因果关系”,“定向传递函数”,“相位-幅度耦合”,“同步可能性(SL)”,“相位滞后指数(PLI)”,“相位锁定值(PLV)”,“幅度包络相关性(AEC)”,“图论”,“集群系数”,“特征路径长度”,“模块化指数”,“线性源估计”,“非线性源估计”,“功能连接性”和“逆问题”。
对于“关心的实验设计”,使用了以下关键词:“纵向研究”(随时间跟踪阿尔茨海默病患者的队列),“横断面研究”(不同严重程度和疾病持续时间的阿尔茨海默病患者样本),“分类研究”(EEG测量在区分对照组、阿尔茨海默病患者和/或其他类型的认知障碍的个体水平的准确性)。
只选取了发表在具有同行评审和影响因子的国际期刊上的文章(-2020年)。有些文章无法从可用的互联网资源下载,因此没有考虑。专家小组的所有选定成员(即C.B.,L.B.,C.D.P.,B.G.,R.L.,F.T.,S. L.,G.N.,和G.Y.)都对所有选定的摘要/论文进行了批判性审查,考虑到Jelic和Kowalski报告的标准;也就是说,原始文章用英语发布,每个诊断组有10人或更多人,按照被用作“金标准”的既定共识临床诊断标准进行诊断。rsEEG测量的有效性主要基于临床神经生理学中rsEEG记录和数据分析的指南。选择的rsEEG论文被区分为三个具有增加权重的任意类别,用于制定建议。如下:
A类:使用AD的CSF或PET诊断生物标志物进行诊断的ADD或ADMCI患者,并且每个组有超过10名参与者。当在A类论文中提供了数据时,我们报告了主要的rsEEG测量结果,以区分AD患者和对照组(见表1、2和3)。
B类:使用传统的AD临床诊断标准作为纳入标准(例如,McKhann等人)并且有较大人群(>100名参与者)的ADD或ADMCI患者,以及认知未受损(CU)的AD和对照组人群。
C类:与B类类似,但人群较小(<100名参与者)。为了简洁起见,在文章中,C类论文没有报告“C类”标签,并且没有提及人数的具体规定。
表1:用于AD临床试验中患者分层的rsEEG节律测量

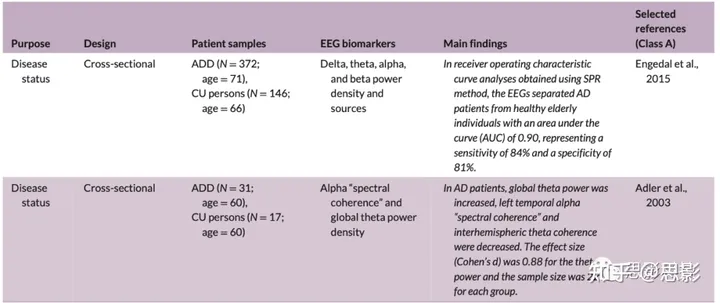
注释:这些生物标志物是指所谓的“A类”交叉和纵向rsEEG研究,其中将ADD、ADMCI或SMC/SCI与老年CU人群(认知完好的CU人群)在安静清醒状态下进行了几分钟的比较。在“A类”研究中,AD患者根据与最新国际指南一致的CSF或淀粉样PET衍生的AD合格生物标志物进行诊断。患者分层可以基于rsEEG测量在组或个体水平上显示AD患者与CU对照个体之间的差异(即包括计算AUROC的分类研究的鉴别准确性)或在随访12个月或更长时间内在其认知下降的统计预测中表现出显著的准确性。请注意,为了测试带有符号“*”的文章发现的普适性,所报告的分类准确性应使用相同(经过训练的)分类器和rsEEG测量在完全独立的来自未参与原始实验的临床记录单位的个体rsEEG数据集中进行交叉验证。rsEEG节律的频带是标准的,即δ波、θ波、α波、β波和γ波。表中更多的文献证据和rsEEG测量的含义(如rsEEG功率密度、“频谱相干性”、产生头皮rsEEG节律的大脑皮层源活动估计等)在正文中有详细描述。当“Class-A”论文中提供的数据可用时,报告了表征AD患者相对于对照组的主要rsEEG测量的效应和样本大小。其他解释和考虑因素在补充信息中报告。
缩写词:AD,阿尔茨海默病;ADD,有痴呆的AD患者;ADMCI,记忆减退的轻度认知障碍;AUROC,受试者工作特征曲线下面积;CSF,脑脊液;CU,认知未受损;HC,健康对照;PET,正电子发射断层成像;rsEEG,闭眼静息状态脑电图;SCI,主观认知障碍;SMC,主观记忆抱怨;SPR,统计模式识别。
表2:用于AD临床试验中患者分层的闭眼rsEEG节律的生物标志物

注释:这些生物标志物是指在随访12个月或更长时间内,在统计预测认知下降方面显示出显著准确性的rsEEG测量。请注意,为了测试具有符号“*”的文章发现的普适性,所报告的分类准确性应使用来自临床记录单位中未参与原始实验的完全独立的个体rsEEG数据集,使用相同(经过训练的)分类器和rsEEG测量进行交叉验证。rsEEG节律的频带是标准的,即δ波、θ波、α波、β波和γ波。表中更多的文献证据和rsEEG测量的含义(如rsEEG功率密度、“频谱相干性”、产生头皮rsEEG节律的大脑皮层源活动估计等)在正文中有详细描述。当“Class-A”论文中提供的数据可用时,报告了表征AD患者相对于对照组的主要rsEEG测量的效应和样本大小。其他解释和考虑因素在补充信息中报告。
缩写词:AD,阿尔茨海默病;ADD,有痴呆的AD患者;ADMCI,记忆减退的轻度认知障碍;AUROC,受试者工作特征曲线下面积;CI,置信区间;CSF,脑脊液;CU,认知未受损;HC,健康对照;PET,正电子发射断层成像;rsEEG,闭眼静息状态脑电图;SCI,主观认知障碍;SMC,主观记忆抱怨;SPR,统计模式识别。
表3:用于监测AD进展和干预措施响应的rsEEG节律测量

注释:这些生物标志物是指“Class A”(请参考表1的定义)的纵向rsEEG研究。这些测量的资格是基于研究结果,在基线与随访记录或药物干预与安慰剂之间存在rsEEG测量差异。例如,在PQ912研究中,ADMCI和ADD患者组成了实验组(n = 60),在12周内接受谷氨酰环化酶酶抑制剂(PQ912),该酶在形成突触毒性的丁二酰胺-A-beta寡聚体中起着核心作用,而安慰剂组(n = 60)在同一期间接受低热量饮料。在其他研究中,ADD和ADMCI患者连续数周/数月接受AChEIs治疗。rsEEG节律的频带是标准的,即δ波、θ波、α波、β波和γ波。当“Class-A”论文中提供的数据可用时,报告了表征AD患者相对于对照组的主要rsEEG测量的效应和样本大小。表中有关rsEEG测量的更多文献证据和含义在正文中有详细描述。
缩写词:AchEI,乙酰胆碱酯酶抑制剂;AD,阿尔茨海默病;ADD,有痴呆的AD患者;ADMCI,记忆减退的轻度认知障碍;AUROC,受试者工作特征曲线下面积;CSF,脑脊液;CU,认知未受损;HC,健康对照;PET,正电子发射断层成像;rsEEG,闭眼静息状态脑电图;SCI,主观认知障碍;SMC,主观记忆抱怨;SPR,统计模式识别。
本文存在一些显著的注意事项和固有限制,包括:(1) 文献综述和分类使用的标准可能具有限制性;(2) 包含了几十年来应用的异质性AD诊断标准的研究,这些标准可能不能排除中度脑血管、非AD海马受损(TDP-43)和Lewy小体共病症的存在,尤其是在老年人中;(3) 头部作为容积传导体对扩散的头皮rsEEG活动的模糊影响(见图4);(4) 初步rsEEG数据分析中检测伪迹的程序存在异质性。
用于AD患者分层的2种rsEEG测量方法
AD患者rsEEG节律的“局部”测量 ADD和ADMCI患者在CSF、神经影像和临床标记物方面,与delta、theta和alpha波段的rsEEG功率密度的线性测量显示出明显的变化。主要结果在下面报告。
在国际多中心的北波罗的海(NORDEEG)研究的两个实验中(A类),与年龄匹配的老年CU人员(n = 138)相比,ADD(n = 117)和ADMCI(n = 138)患者表现出全局theta功率密度增加和认知性能下降,以及后部alpha-beta功率密度与认知性能之间的正相关性。此外,CSF Aβ42的减少显著与在所有电极上平均的theta和delta功率密度的增加(全局场功率[GFP])有关,这在被诊断为主观认知下降(SCD, n = 210)、MCI(n = 230)和ADD(n = 197)的患者中都得到了证实。相比之下,增加的p-和t-tau与alpha和beta GFP的减少有关。此外,CSF Aβ42的减少和p-和t-tau的增加显著与在所有电极上的alpha和beta全球场同步化(GFS)的减少有关,这与认知状态有关。
欧洲多中心的PHARMACOG研究(A类)比较了记忆型MCI老年人的rsEEG测量和诊断性CSF标记物,这些标记物与AD诊断不兼容(noADMCI,n = 54)和兼容(ADMCI,n = 72)。统计模型整合了每6个月进行一次的记录结果,持续2年的rsEEG源估计。结果显示,与no ADMCI患者相比,ADMCI患者的特点是全局delta和theta源活动增加,后部delta-theta和alpha源活动的比例增大。此外,能够在最后的随访中被评估的ADMCI患者(n = 63)表现出枕部theta/alpha源活动与全球认知状态之间的关联,通过阿尔茨海默病评估量表-认知分量表分数进行测量,并且在静息状态功能MRI标记中,默认模式网络的连通性减少。
在意大利-土耳其 rsEEG 研究(A 类)中,与正常老年认知正常(CU)者相比(n = 60),教育水平较高的ADMCI患者(n = 35)在整个脑区显示出较高的α波源活动。与之相反,与教育水平较低的ADMCI亚组相比,教育水平较高的ADMCI亚组显示出更广泛的低α波源活动(值得注意的是,这两个ADMCI亚组具有匹配的脑脊髓液AD诊断生物标志物、载脂蛋白E [APOE] ε4基因型、脑灰白质测量和神经心理评分)。
Jeong的另一项研究(A类)研究了CSF生物标记物和AD患者(n = 14)EEG参数之间的关联。这些患者在CSF Aβ42浓度和theta波段右侧颞区电流源密度对数之间显示出显著的负相关。总tau浓度与AD患者alpha-2波段左侧额眼野和右侧听觉区之间的滞后相位同步性负相关。
AD神经病理学对delta、theta和alpha节律幅度的影响得到了以下独立全球协作组的研究的支持(B类)。
在一项基于NEWYORK(n = 264)和STOCKHOLM(n = 155)rsEEG数据库的研究中,与认知完好的CU个体相比,ADD和ADMCI患者的特征是alpha、beta和gamma GFS降低,delta GFS增加。在另一项STOCKHOLM rsEEG研究中,与ADMCI(n = 31)和年龄匹配的CU人员(n = 24)相比,ADD(n = 38)患者显示出alpha和beta GFP(全局场功率)降低,以及头皮alpha和beta节律的偶极源位置前移。
在一些ITALIAN rsEEG研究的实验中,与CU人员(n = 126)相比,ADD(n = 193)和ADMCI(n = 155)患者在认知性能方面,呈现出delta源活动的广泛增加和后部alpha源活动的减少,这是通过Mini-Mental State Evaluation(MMSE)评分和其他神经心理测试揭示的。此外,这些rsEEG源活动的异常与结构(例如,海马和皮质灰质萎缩)和功能(例如,后部皮质区FDG-PET代谢不良)神经影像标记物有关。在源级别的发现得到了头皮级别的GFP标记物的交叉验证。实际上,ADMCI患者(n = 85)显示出theta和gamma功率密度的比例,以及高频和低频alpha功率密度的比例,与认知状态相关的海马、丘脑和基底节灰质萎缩有关。
在欧洲DESCRIPA rsEEG研究中,与非遗忘型MCI(n = 51)、SMC(n = 53,未对大脑中的淀粉样沉积进行测试)和年龄匹配的CU(n = 79)人员相比,ADMCI患者(n = 92)表现出枕部-额部theta源活动增加和后部alpha源活动减少。
在Roh等人的研究中,与CU人员(n = 39)相比,ADD(n = 41)和ADMCI(n = 38)患者呈现出(1)更高的颞部和枕部-顶部theta功率密度和后部alpha源活动的减少;(2)相对于认知缺陷,顶部-枕部alpha和额部和颞部beta 功率密度降低。
其他C类rsEEG研究显示,关于delta、theta和alpha功率密度与认知功能的关系,结果类似。
此外,beta功率密度(13-25 Hz)与ADD患者的良好认知功能呈正相关。
B类和C类的其他研究探索了rsEEG功率密度和ADD患者神经影像测量之间的关系。与年龄匹配的CU人员相比,ADD患者显示出异常的静息状态功能MRI连通性,以及通过99mTc-HMPAO SPECT或FDG-PET扫描,分别显示出区域皮质血流和或新陈代谢的减少,这与空间广泛的delta功率密度或皮质源活动有关(C类:Stigsby等人;B类:Brenner等人;B类:Rae-Grant等人;C类:Kwa等人;C类:Rodriguez等人;C类:Peraza等人)
2.1.1 年龄和遗传风险因素
如下述rsEEG研究(B类)所示,上述效应受到年龄和遗传风险因素的调节,而性别因素被匹配或用作协变量。在VU阿姆斯特丹大学医学中心(AMSTERDAM研究)的rsEEG研究中,ADD(n = 320)和认知完好(n = 246)的老年人中,年轻(≤ 65岁)比老(> 65岁)的人delta和alpha功率密度的异常更为明显。
在ITALIAN rsEEG研究中,与年龄匹配的CU人员(n = 89)相比,ADMCI患者(n = 84)的后部alpha源活动较低,尤其是在携带半胱天冬酶C基因型B型的患者中。在APOE ε4基因型非携带者中,也观察到ADMCI(n = 89)和ADD患者(n = 103)的后部alpha源活动有类似的影响。这种效应在使用类似方法的独立研究中被复制,在ADD(n = 125)和CU人员(n = 60)中。然而,这在AMSTERDAM研究中并未被复制,该研究使用了基于头皮rsEEG功率密度测量的方法论方法,对ADD(n = 320)和CU人员(n = 246)进行了研究。
上述rsEEG测量(例如,delta-theta功率密度增加和后部alpha功率密度减少)在其他研究中的ADD和ADMCI患者中有所不同,如下述研究(B类)所报告。与年龄匹配的CU人员(n = 35)相比,ADD患者(n = 61)以头皮delta功率密度广泛异常为特征。
欧洲Lewy体痴呆联合体(E-DLB研究)进行了一项rsEEG研究,包括CU(n = 42)和ADD(n = 42)患者。结果显示,AD患者的后部alpha源活动异常较大,delta源活动异常较少。
在ITALIAN研究中,ADD(n = 60)的delta和theta GFP(全局场功率)比年龄相符的CU人员(n = 30)更高,而alpha GFP较低,这与之前的相关证据一致。此外,与年龄相符的CU人员(n = 38)相比,ADD患者(n = 48)表现出后部alpha源活动的减少和空间广泛的delta源活动的增加。
在另一项rsEEG研究中,ADD患者(n = 62)的alpha与delta+theta功率密度之比,以及全球rsEEG平均频率,都低于CU人员(n = 14)。
2.1.2 临床前AD
先前的rsEEG研究在脑淀粉样物质沉积显著的SMC老年人(临床前AD神经病理学)中表现出混合结果。
在法国INSIGHT-preAD研究(A类)中,年龄在70至85岁之间的SMC老年人(n = 318)通过18F-florbetapir PET标准化摄取值比(SUVR)进行了测试,以作为脑部淀粉样沉积的标志,并进行了广泛的数据收集,包括rsEEG记录。有三篇文章报告了rsEEG的发现。在第一项研究中,淀粉样沉积与后部α波功率密度之间存在负向趋势(β波功率密度无影响)。在第二项研究中,结果显示AD病理与δ、β和γ波的功率密度之间存在非线性的U型关系,而与α节律的关系仍不清楚。
在第三项研究中,AD病理和教育水平较高与后部α波功率密度有关(其他标准频带无影响)。综合这些发现,这些结果表明临床前期AD病理可能会影响SMC老年人的rsEEG节律,但对后部α节律或其他rsEEG指标的影响不确定。
2.1.3 非线性rsEEG测量
在INSIGHT-PreAD项目(A类)中,与大脑中没有明显淀粉样沉积的SMC老年人(n = 175)相比,具有临床前AD神经病理学(n = 25)的个体显示出通过FDG-PET代谢减退显示的神经退行性与额中央β和γ频率功率密度增加、δ频率功率密度减少、频谱熵升高、复杂度增加以及在θ节律中通过加权符号互信息测量的功能连接性增加相关。有趣的是,如果神经退行超过一定的淀粉负荷阈值,rsEEG指标的整体趋势将逆转,δ功率增加,以下变量减少:β和γ功率、中位数频谱频率、频谱熵、复杂度等,这些通常是ADMCI和ADD的特征
大部分先前的研究显示了CU个体和ADD患者在电极对的rsEEG节律的“相互关联性”或皮层源连接度估计方面的差异的收敛证据。其中许多研究使用了电极对的“频谱相干性”,这是一种非常流行的线性rsEEG技术。与年龄匹配的CU个体相比,ADD患者在α(8-12 Hz)和β(13-20 Hz)节律的电极对之间表现出较低的“频谱相干性”。 然而,这些效应在脑图上是可变的,在一些研究中观察到颞顶枕电极对和额中央以及额顶枕电极对中。
在AMSTERDAM研究(B类)中,与年龄匹配的CU个体相比,ADD(n = 109)和ADMCI(n = 88)患者的全局α和β节律的“同步可能性”(对线性和非线性“相互关联性”敏感)较低。 此外,ADD患者在与疾病严重程度相关的全局α“相位滞后指数”方面表现出降低。
在同样的研究方向上,意大利多中心rsEEG研究(B类)报告了ADMCI患者(n = 57)中全局α“频谱相干性”的降低,这与基于MRI显示的来自基底前脑到大脑皮质的胆碱能通路的脑血管损害有关。这些效应在与CU(n = 69)相比的ADD(n = 109)、VaD(n = 25)和ADMCI(n = 88)患者中被空间指定。ADD和ADMCI患者与CU个体相比,在额顶部α节律的“同步可能性”方面显示出减少。此外,“定向传递函数”(DTF;一种基于格兰杰因果性导出的多变量rsEEG“相互关联性”测量)在从顶部到额部电极的传输中显示出ADD和ADMCI患者低于年龄匹配的CU个体。这一效应在独立的调查中得到了证实。
在一项单中心rsEEG研究(B类)中,与年龄匹配的CU个体(n = 60)相比,另一种与“频谱相干性”相关的测量方法(即“相位同步”)显示出ADD患者(n = 125)在颞叶和顶叶电极之间的α节律“相互关联性”降低。
在欧洲E-DLB研究(B类)中,另一种称为“线性滞后连接度”的rsEEG测量(消除对头容导电效应更敏感的零滞后“相互关联性”)显示ADD(n = 120)和ADMCI患者(n = 70)之间广泛降低的α半球间α节律源连接性,与年龄匹配的CU个体(n = 100)相比。
AD对上述rsEEG“相互关联性”的影响在δ(< 4 Hz)和θ(4-7 Hz)频段上不太明确。与年龄匹配的CU个体相比,ADD患者在低频率上显示出降低的“频谱相干性”,尤其是在中央θ节律上。 相反,其他的rsEEG研究报道了δ节律上“频谱相干性”的普遍增加,或者呈现出在不同电极对上的“频谱相干性”值增加和减少的相当复杂的地形模式。
具体而言,Sankari等人观察到(1)左半球前额叶在α、θ和δ节律中的内半球内部相干性增加,(2)所有频段中左半球颞顶联合相干性增加,以及(3)所有频段中右半球颞顶中央区的内半球相干性降低。
其他rsEEG“相互关联性”的测量结果如下:
在一项大型单中心rsEEG研究(B类)中,与CU个体(n = 60)相比,ADD患者(n = 125)的全局θ节律“相位同步”较高。
在意大利的rsEEG研究(B类)中,“线性滞后连接度”显示出ADD患者(n = 120)在枕叶源处的δ频段半球间连接性增加,以及在枕叶-颞叶源处的θ频段半球内连接性增加,与年龄匹配的CU个体(n = 100)相比。 而“同步可能性”显示出在δ频段上,ADD(n = 82)和ADMCI患者(n = 88)与CU个体(n = 69)相比,相互关联性普遍增加。
相反地,一项全国单中心rsEEG研究显示,在ADMCI患者(n = 9)与年龄匹配的CU个体(n = 14)之间,在前额叶内部和前额叶与颞/顶叶电极之间的δ和θ节律上,"相位滞后指数"(消除零滞后相干性的影响)呈现降低。
上述研究中的一些不同结果可能是由于应用了不同的rsEEG“相互关联性”测量方法(“频谱相干性、同步可能性、相位滞后指数、滞后连接度、DTF”)以及它们对容积效应和共同驱动效应的不同敏感性所致(有关更多讨论,请参阅支持信息中的AD研究中使用的rsEEG测量的主要特征,图S1)。

图 S1. 头部容积传导、"共同驱动"、和"级联流"的效应对rsEEG节律的功能和有效连接计算技术的结果解释产生混淆的一些示例。
上方行:基于一个包含三个探测头皮电极 "a","b" 和 "c" 以及四个潜在皮层源 "At"(即位于电极 "a" 下方,具有切向取向),"ABr"(即位于电极 "a" 和 "b" 之间,具有径向取向),"Br"(即位于电极 "b" 下方,具有径向取向)和 "Cr"(即位于电极 "c" 下方,具有径向取向)的模型的一些示例。在该模型中,源 "At" 的电场通过容积传导到电极 "b"。源 "ABr" 的电场通过容积传导到电极 "a" 和 "b"。源 "Br" 的电场通过容积传导到电极 "b"。源 "Cr" 的电场通过容积传导到电极 "c"。在这个模型中,电极 "b" 记录了由皮层切向源 "At" 和皮层径向源 "ABr" 和 "Br" 产生的电场。由于皮层源定位/取向和头部作为容积传导体的效应,收集在给定探测头皮电极处的 EEG 信号的相位和幅度将反映皮层源与其相对距离的加权平均贡献。实际上,来自皮层源的电场在 10-12 厘米的距离处衰减到零值,由于头部和源几何形状,距离超过 20 厘米可能还会有轻微的额外效应[21]。值得注意的是,头部容积传导效应的影响因潜在皮层 EEG 源的扩展而放大。在所有频率带中,记录在给定头皮电极处的 EEG 活动可能反映分布在数十平方厘米的广泛皮层区域的同步皮层源[20]。在图中的理想模型中,丘脑皮层神经群体可能的同步影响没有显示。此外,探测头皮电极 "a","b" 和 "c" 处的 EEG 活动(未显示)将相对于一个远离的参考电极(未显示)进行记录。
中间行,左侧。由于头部容积传导,源“ABr”的激活可能导致在电极“a”和“b”处记录的rsEEG节律的相互依赖。这种相互依赖可能会被错误地解释为潜在这些电极的皮层源“At”和“Br”之间的功能连接。
中间行,右侧。由于头部容积传导的效应,源“At”和“Cr”的协同激活可能导致在电极“b”和“c”处记录的rsEEG节律的相互依赖。这种相互依赖可能会被错误地解释为潜在这些电极的皮层源“Br”和“Cr”之间的功能连接。
下方行,左侧。由于“共同驱动”的效应,源“Cr”与源“Br”和“ABr”的协同激活可能导致在电极“a”和“c”处记录的rsEEG节律以及在电极“b”和“a”处记录的节律之间的相互依赖。这种相互依赖可能会被错误地解释为潜在这些电极的皮层源“At”和“Cr”以及皮层源“Br”和“ABr”之间的功能连接。
下方行,右侧。图中展示了从源“Cr”到“Br”以及从“Br”到“ABr”的定向连接,以显示“直接”和“间接”连接路径之间的区别。在图中,从源“Cr”到源“Br”有一个“直接”的连接路径,而源“Cr”和“ABr”之间的连接路径是“间接”的。在图中,源“Br”还显示了到源“ABr”的定向连接。由于“级联流”效应,这种源连接模式可能导致在电极“c”和“a”处记录的rsEEG节律的定向相互依赖。在头皮传感器上,对该相互依赖的两个错误解释会推断出源“Br”和“ABr”之间以及源“Cr”和“At”之间的功能连接。
在图中,头皮电极之间的绿色箭头表示传感器级别的EEG活动(未显示)的相互依赖,这对应于潜在皮层源之间的功能连接,也由绿色箭头表示。在这种情况下,这种相互依赖揭示了真正的潜在功能性皮层连接。相比之下,头皮电极之间的红色箭头表示头皮层面的EEG活动(未显示)的相互依赖,这不对应于潜在皮层源之间的功能连接,也由红色箭头表示。在这种情况下,这种相互依赖提供了对潜在功能性皮层连接的误导性表示。
局部和相互关联性”的rsEEG节律测量在AD个体分类中的应用
rsEEG测量可以用于量化ADD和ADMCI个体的脑神经生理功能障碍,以在观察性和干预性临床试验中对其进行亚组分层。基于rsEEG测量对AD和对照个体进行区分的分类率>80%。
在NORDEEG研究(A类)中,颞叶θ节律功率密度在ADD(n = 117)和CU个体(n = 138)之间的区分中显示了73%的分类率。在同一研究中,结合了α和θ的GFP在ADD(n = 38)与CU(n = 24)个体之间的区分中达到了84%,以及在ADD和ADMCI患者之间的区分中达到了78%。此外,结合左侧颞-枕电极(T5-O1)的α和θ相对功率密度以及平均频率,可以以85%的准确性正确预测ADMCI(n = 27)患者的痴呆进展。
在AMSTERDAM研究(A类)中,使用全局rsEEG功率密度、成对的“相互关联性”(“相位传递熵”)以及多个频段上的最小生成树图指标来训练随机森林学习机(即最高度、叶节点数和树层次),以区分ADD(n = 66)和年龄匹配的CU个体(n = 66)。这种方法在区分CU个体和ADD个体之间的分类准确性达到了62%。
在意大利的rsEEG研究(B类)中,颞顶-枕部位δ和α皮层源活动之间的比值在区分ADD(n = 127)和年龄匹配的CU个体(n = 121)时,ROC曲线下面积达到了75%。这些结果的临床意义还通过在所有CU和AD受试者的整体组中,对颞顶-枕部位皮层δ或α1源活动与MMSE评分之间进行相关性分析来进行了测试。结果显示,颞顶-枕部位δ源活动越高,MMSE评分(即全局认知状况)越低。此外,优势颞顶-枕部位α1源活动越高,MMSE评分越高。
此外,对图小世界性指数进行一阶多项式回归在区分稳定的ADMCI患者(n = 74)和进展的ADMCI患者(n = 71)之间达到了61%的ROC曲线下面积,考虑到APOE ε4等位基因后,准确率达到了97%。
在E-DLB rsEEG研究(B类)中,δ和α皮层源估计在区分年龄匹配的CU个体和ADD患者(每组n = 42)方面,ROC曲线下面积达到了85%至90%。83 在对AD的前驱期(即MCI)阶段的个体(n = 75)进行分类时,这种准确性下降至80%以下。
这些发现扩展了其他较小的国家级rsEEG研究的结果。在电极对之间的全局δ和α“频谱相干性”成功地将ADD患者(n = 64)与CU个体(n = 54)进行分类,分类准确率>80%。136 此外,逐步逻辑回归分析使用左侧颞叶α“频谱相干性”和全局θ功率密度在ADD患者(n = 31)和CU个体(n = 17)之间达到了82%的分类准确率。
一项重要的国家级研究(B类)从方法学的角度来看非常重要。该研究使用了两个rsEEG数据库,一个由ADMCI(n = 25)和CU(n = 56)个体组成, 另一个基于ADD(n = 17)和CU(n = 17)个体。在第一个实验中,使用均方和相位相干性、格兰杰因果原理(例如,局部相干性、DTF、直接DTF、全频DTF)、相位同步指数、信息论差异、基于状态空间的指数和随机事件同步(SES)i进行比较,以区分ADMCI和CU个体。大多数同步度量指标表明MCI患者的脑电同步减少。然而,这种效应在只有两个指标(ffDTF和SES方法的ρ)上是统计学上显著的。SES方法通过线性判别分析和二次判别分析分别达到了68%和75%的分类准确率。相反,ff-DTF方法通过线性判别分析和二次判别分析均达到了70%的分类准确率。组合测量达到了83%的分类准确率。
在第二个实验中,使用ADMCI和ADD患者,ff-DTF和SES分别达到了83%和98%的分类率。其他国家级单中心研究复制了这些结果,在θ和α节律上使用这些程序的组合可以在AD和对照CU个体之间达到90%以上的准确率。
在欧洲DECIDE rsEEG研究(B类)中,非归一化的DTF和频谱相干性主要结合了δ、θ和α节律,在区分ADD和对照CU个体时,ROC曲线下面积达到了86%到88%。
Bennys等人报道,通过计算绝对功率EEG波段中枕叶-颞叶-顶叶的θ频段与α+β频段之间的比值,可以在ADD(n = 35)和年龄匹配的CU(n = 35)个体之间的区分中达到86%的ROC曲线下面积,轻度受损患者中快速活动明显减少。
通过使用基于学习分类器的更先进的数学分类器进行验证(请参阅支持信息中的分类研究中“夸大”的区分准确性的注意事项),以下大型国家级单中心rsEEG研究(B类)的结果得到了证实。
通过将人工神经网络作为分类器,在痴呆患者(n = 111)和年龄匹配的CU个体(n = 56)之间的区分中,使用绝对δ和θ功率密度的地形分布作为输入rsEEG测量,获得了90%的分类率。此外,通过将rsEEG功率密度和“相互关联性”测量作为多个数学分类器(包括主成分线性判别分析、偏最小二乘线性判别分析、主成分逻辑回归、偏最小二乘逻辑回归、装袋法、随机森林、支持向量机和前馈神经网络)的输入,达到了类似的区分准确率,使用最佳结果,随机森林在轻度ADD患者(n = 116)和年龄匹配的CU个体(n = 45)之间的区分中达到了81.5%的分类准确率,而神经网络在中度ADD(n = 81)和CU个体之间达到了88.5%的分类准确率。
在意大利的rsEEG研究(B类)中,使用多通道rsEEG电压时间序列作为输入,通过先进的“IFAST”人工神经网络对ADD(n = 180)、ADMCI(n = 115)和CU个体(n = 171)进行了区分。这种方法在ADD和CU个体之间以及ADD和ADMCI患者之间显示出超过90%的分类准确率。基于基线和1年临床随访记录的rsEEG节律(0-12 Hz),ADMCI患者在回顾性分类中以86%的准确率进行了分类,区分那些进展到ADD的患者和那些具有稳定ADMCI状态的患者。值得注意的是,使用最具有区分能力的皮层源活动(例如相对于δ/θ源的后部α)作为反向传播人工神经网络的输入,并没有改善分类准确率(77%的准确率)。
在其他研究中,基于Sugihara因果分析的新型rsEEG“相互关联性”测量在CU(n = 15)、MCI(n = 16)和ADD(n = 17)个体(C类147)以及基于区域间转移熵分析在CU(n = 15)、MCI(n = 16)和ADD(n = 17)个体(C类148)中获得了94%至98%的高分类准确率。
在NORDEEG研究中(A类),采用支持向量机作为统计模式识别(SPR)的步骤性分类程序,根据从原始EEG记录中提取的20个选定的rsEEG测量(即功率密度和“频谱相干性”)为每个人生成了从0到1的五个值。这五个值对应以下诊断标签:“NRM”(CU个体指数)、“sMCI”(MCI指数)、“AD”(AD指数)、“ADms”(AD,中度/重度指数)和“LP”(Lewy体痴呆/帕金森病指数)。一个图形在其置信区间内表示这些值,以支持诊断。一项开创性的实验测试了仅基于该基于EEG的图形进行评估的临床医生的诊断准确性,使用由经验丰富的多学科团队根据至少两名经验丰富的医师(专业级别的痴呆症专家)的一致意见获得的临床诊断作为金标准。该团队使用所有可用的检查结果(例如临床、神经心理学、液体生物标志物、神经影像标志物)独立地(“盲目”)给出临床诊断,而不考虑EEG结果。涉及五个使用协调的EEG程序的临床单位。该程序用于对接受脑脊液诊断生物标志物评估的ADD(n = 32)、MCI(n = 56,其中65%的患者脑脊液诊断生物标志物值与AD兼容)和CU个体(n = 41)进行诊断。基于EEG图形的诊断准确性以正确诊断的百分比表示,将所提及的临床诊断作为金标准。结果显示,基于EEG图形的相对较低-中等的诊断准确性为:ADD与MCI的诊断准确性为60%、ADD与CU的诊断准确性为66%、MCI与CU的诊断准确性为56%。
在此先例中,相同的研究组织在更大的人群中开展了其他实验(B类),并非所有个体都接受了脑脊液诊断生物标志物分析。在一项有趣的实验中,基于上述0到1的SPR指数,对CU个体(n = 146)、ADD(n = 135)和LP(n = 15)的老年人进行了正确分类的准确性测试。SPR指数被用作ROC曲线分析的输入。结果显示了以下正确的二元分类结果:ADD(n = 135)与CU(n = 146)个体的准确性为90%。这些研究结果优于基于标准的神经影像的视觉评估进行的同一分类实验,并与在相同的NORDEEG队列中应用相同的分类程序进行的ADD(n = 226)、ADMCI(n = 41)和CU个体(n = 226)的先前证据相一致。使用基于支持向量机的独立SPR程序在CU个体和痴呆患者的小人群中也得到了类似的结果。
在个体水平上考虑上述rsEEG结果时,跨rsEEG频带结合“同步性”和“关联性”测量可以反复产生ADD和ADMCI与对照CU个体之间的二元分类,准确率在70%至90%之间,因此在AD临床试验中可能有用于患者分层的目的。值得注意的是,将这些二元分类用于单模态诊断目的时,提供的准确性较低,约为60%。
在比较ADD/ADMCI患者和对照CU个体时,流行的图论方法研究了rsEEG节律的“关联性/功能连接”的拓扑结构(另见Tijms et al.的综述)。
与年龄匹配的CU个体相比,ADD和ADMCI患者在电极或源对的rsEEG“关联性”拓扑结构上表现出更随机的特征,可能是由于基础皮质神经网络的“小世界性”特性的减少。然而,需要指出的是,支持这种解释的rsEEG研究对构成“小世界”的单一图指标(即“聚集系数”和“路径长度”)的结果存在不一致,并且对δ、θ、α、β和γ波段的影响不明确。这种不一致性可以部分解释为(1)这些研究中使用了不同的rsEEG“关联性”测量方法;(2)应用了比多元测量方法更容易受到容积传导和共同驱动效应影响的双变量测量方法(请参见支持信息);(3)使用传感器级别与源级别;以及(4)使用不同的统计阈值。
除了小世界性,还测试了其他图指标(见方框2中的定义)。在英格兰东北地区的NORTH-EAST ENGLAND研究中(A类),使用rsEEG节律的“相位滞后指数”在电极对之间的最小生成树(MST)来模拟皮质网络的分层聚类组织作为rsEEG“关联性”的拓扑结构,比较了对照CU个体(n = 17)和ADD患者(n = 26)。与年龄匹配的CU个体相比,ADD患者显示出较低的α节律“相位滞后指数”和较低的主导频率(α范围的最大rsEEG功率密度)。
在AMSTERDAM研究中(B类),同样使用了基于电极对的rsEEG节律的“相位滞后指数”的MST来模拟ADD(n = 133)和CU个体(n = 115)之间的rsEEG“关联性”的拓扑结构。与年龄匹配的CU个体相比,ADD患者在疾病严重程度增加时表现出α节律“相位滞后指数”的降低,并且“节点”的“中介中心性”质心从后部向前部头皮区域转移。对于这些结果的特异性,额叶δ节律“相位滞后指数”在行为变异性额颞型痴呆患者(n = 48)中被选择性地受到影响,而在保持“全局效率”不变的背景下,ADD患者(n = 69)观察到了顶叶和枕叶网络组织和“全局效率”的损失,与α节律“相位滞后指数”的降低有关。
在考虑上述结果的基础上,rsEEG节律的“关联性”的图拓扑结构可能丰富我们对AD作为一种“失联”综合征的理解。然而,用于在AD临床试验中系统应用的最一致的地形模式和rsEEG测量尚未确定。需要进行更多的国际研究,以改进基于多变量模型和源估计的计算rsEEG活动的“关联性”的有前景的技术。
在CU人群和AD患者中的先前纵向研究中,测试了基线数据集中派生的rsEEG测量指标对预测其随访期间的认知状态的价值。
在AMSTERDAM rsEEG研究中(A类),高的δ-θ节律和较低的α节律功率密度预测了SCD患者(n = 63)和脑部淀粉样沉积的MCI患者(n = 142)随时间的临床恶化。
在STOCKHOLM rsEEG研究中(A类),来自左侧颞-枕区域的α和θ节律功率密度和平均频率预测了ADMCI患者(n = 27)在1年随访期间的认知衰退。在一项平行的rsEEG研究中,α源的前置定位预测了ADMCI患者(n = 31)在约2年的随访期间的认知衰退。
在另一项国家级rsEEG研究中(B类),低后置α节律功率密度预测了ADMCI(n = 88)和ADD(n = 42)患者在1年随访期间的认知衰退。
在ITALIAN rsEEG研究中(B类),ADMCI患者(n = 74)在头皮电极处具有较高的α3/α2频率功率密度比值,显示出颞顶叶皮质的更大萎缩和较低的灌注率,并在3年随访期间转变为ADD状态。此外,高颞部δ源活动预测了ADMCI患者(n = 69)在平均14个月的随访期间的显著认知衰退。
在NEWYORK rsEEG研究中,高颞顶叶θ节律功率密度和平均rsEEG频率减慢预测了SMC患者(n = 44)在7至9年的随访期间从轻度认知障碍进展为明显认知缺陷,总体预测准确率达到90%,从而扩展了该工作组在CU人群、SMC、ADMCI和ADD个体中的先前证据。
在另一项国家级rsEEG研究中,基线时期高θ节律功率密度和认知表现预测了CU人群(包括认知完好的个体(n = 24)和ADMCI(n = 20)、ADD(n = 14)患者)在平均20个月的随访期间的认知衰退,总体预测准确率达到93%。
表1和表2列出了本章中回顾的A类rsEEG研究中最一致的发现。它们支持了使用“大脑皮层神经同步”和“相互关联/连接性”的rsEEG测量指标对AD状态进行表征以及对患者在临床试验中进行认知衰退预测的重要价值,以用于患者的分层。
3个反映AD进展和干预效果的rsEEG节律测量指标
ADMCI和ADD患者中疾病进展的rsEEG测量价值
针对AD和CU个体进行的多项研究测试了rsEEG测量在监测脑功能障碍进展方面的价值,比较了基线和随访记录得出的这些测量指标。以下是核心结果:
在斯德哥尔摩rsEEG研究中(A类),ADMCI(n = 27)的老年人在平均21个月的随访中显示出颞叶和枕叶θ-δ节律功率密度增加以及β节律功率密度减少。48
在国际多中心PHARMACOG rsEEG研究中(A类),与无ADMCI患者(n = 54)相比,ADMCI患者(n = 72)在24个月的随访期间表现出增加的边缘系统θ节律源活动,并且在休息态功能性磁共振成像揭示的皮层默认模式网络内功能连接性减少的情况下认知能力下降更为明显。
在意大利rsEEG研究中(B类),与年龄匹配的CU个体(n = 35)相比,ADD患者(n = 88)在平均13个月的随访中显示出δ节律增加以及顶枕区α和β节律源活动减少。在同一研究中,在ADMCI的前驱阶段也观察到了类似的效应。具体而言,ADMCI患者(n = 55)在平均13个月的随访中显示出后部区域α节律源活动减少。
其他关于AD和对照组CU个体的国内单中心研究测试了rsEEG测量指标在监测进行性脑功能障碍中的价值。在平均30个月的随访中,ADD患者(n = 40)表现出顶枕区θ-δ节律功率密度增加和α-β节律功率密度降低。在另一项研究中,半数的ADD患者(n = 40)表现出平均12个月的随访中颞叶和枕叶δ-θ节律功率密度增加。 另一项研究中,ADD患者在平均2年的随访中显示出δ-θ节律功率密度增加和α节律功率密度降低,而VaD和功能性精神病患者未观察到变化。最后,rsEEG节律的“相位滞后指数”测量显示AD患者脑功能障碍的进行性。与年龄匹配的CU个体(n = 14)相比,ADMCI患者(n = 9)在1年随访中显示出额叶内和额叶与颞/顶区之间的δ和θ节律“相位滞后指数”降低。
几项国内研究探讨了乙酰胆碱酯酶抑制剂(AChEIs)对ADD患者的rsEEG测量指标的影响,这些药物可以增强乙酰胆碱能系统的功能。
在斯德哥尔摩rsEEG研究(A类)中,与未接受治疗的ADD患者相比,接受AChEIs(他克林)治疗的AD患者(n = 15)在治疗3个月和12个月后的θ节律GFP有所减少,而在治疗6个月后δ和θ节律GFP均有所减少(n = 10)。这些结果扩展了先前的证据。
在德国研究(B类)中,rsEEG测量指标对AChEIs在ADD患者中的敏感性得到了验证。在一组AD患者(n = 15)中,α-θ节律功率密度比在单剂AChEIs(四氢氨基吡啶)后对慢性治疗(7周)的临床效果进行了预测。在其他ADD患者(n = 15)中,在接受AChEI(雷吡舒胺)治疗5天后观察到广泛的δ和θ节律功率密度显著降低,而在治疗1至2周后(雷吡舒胺),只观察到θ节律功率密度降低(n = 35)。在另一组ADD患者(n = 20)中,治疗1周后降低的θ节律功率密度和短期记忆表现能够预测6个月随访时的治疗反应(雷吡舒胺)。
在意大利的rsEEG研究中(B类),与CU个体(n = 65)相比,ADD患者(n = 58)在1年的随访中显示出后部α节律源活动的降低。对于同时接受AChEIs(多奈哌齐)辅助治疗的患者(n = 28),相对于未作出反应的患者(n = 30),其整体认知状态(即MMSE分数)显示出较小的改善。
其他较小的国内rsEEG研究报告了ADD患者中类似的效果。具体来说,AD患者(n = 18)在服用AChEIs(多奈哌齐)治疗6个月后,显示出颞区δ节律功率密度显著降低以及其他频率范围(包括颞区和中心顶区)的功率密度增加。这个效果与其他证据一致。此外,另一组ADD患者(n = 16)在服用AChEIs(雷吡舒胺)治疗3个月后,广泛的δ和θ节律功率密度显著降低。对这些数据进行皮层源定位表明在网络中出现显著影响,包括左侧额顶区、后扣带回皮层、双侧海马旁区和海马。
ADMCI和ADD患者的其他药物干预措施也对rsEEG测量指标产生显著影响。核心结果如下所述。
在PQ912研究中(A类),ADMCI和ADD患者组成了一个实验组(n = 60),接受了为期12周的谷氨酰环化酶(PQ912)抑制剂治疗。该酶在突触毒性的焦谷氨酸-A-beta寡聚体形成过程中起着核心作用,而安慰剂组(n = 60)在同样的时间内接受低热量饮料。结果显示,与安慰剂组相比,实验组的记忆力有所改善,theta GFP降低。值得注意的是,PQ912干预对作为rsEEG“互相关性”的测量指标的“相位滞后指数”没有影响。在对这些rsEEG数据进行重新分析时,实验组(n = 47)在alpha频带上的电极对之间的rsEEG“互相关性”新测量指标(包括带泄漏校正的幅度包络相关性,AEC-c)的增加程度大于安慰剂组(n = 56)。
在国际SOUVENAID II研究中(B类),ADD患者组成了一个实验组,在24周内接受SOUVENAID功能性食品治疗(n = 86),而安慰剂组在同样的时间内接受低热量饮料(n = 93)。结果显示,与安慰剂组相比,SOUVENAID组的记忆力有所改善,并且在所有电极对中全局delta“相位滞后指数”增加。对“相位滞后指数”数据的重新分析表明,在实验组的一个子样本(n = 70-66)中,24个月随访期间的beta节律的局部脑网络连接保持稳定,而安慰剂组(n = 77-75)没有。
表3报告了本章所述的A类rsEEG研究的最一致结果。它们支持rsEEG测量在AD进展和药物干预的临床试验中的价值。
在文献综述中,AD患者表现出最一致的异常是(闭眼)rsEEG节律的变化,表现为头皮电极上的δ-θ和α频段功率密度的改变,或者是对皮层源活动的估计。可以推测,这些异常可能直接或间接地反映了AD病理对涉及皮层rsEEG节律生成和大脑唤醒、皮层抑制/兴奋平衡和警觉调节的分布式脑神经网络的影响。这些网络可能由亚皮层和皮层神经回路组成,而且在主动事件相关信息处理期间,丘脑皮层功能连接具有特殊作用。然而,越来越多的文献涉及AD病理与β和γ节律的关系。最近的研究显示,一旦淀粉样物负荷超过一定水平,β和γ频段的功率谱水平明显降低。其他研究结果表明,γ功率以及γ相干性在AD患者中明显受到影响。有关rsEEG研究中所述发现的神经生理基础的更多讨论可在支持信息中的《AD患者异常rsEEG测量的生理基础》中找到。
5.建议
单独的rsEEG测量在诊断中的特异性 尽管有过历史性的努力进行基于证据的综述,但rsEEG测量的诊断效用仍存在争议。Jelic和Kowalski使用基于证据的技术,对1980年至2009年发表的有关认知障碍性疾病的rsEEG诊断准确性的文献进行了系统综述。他们得出的结论是,尽管分类准确性值通常较高(>80%),但有关rsEEG标志物在AD中的诊断效用的证据还不足以建议其单独在记忆门诊常规中使用,还需考虑到它们不能直接测量潜在的AD神经病理。同样,在AD诊断的国际指南中,也未推荐使用rsEEG生物标记作为诊断目的;相反,它们针对的是AD神经病理的分子和结构测量。值得注意的是,本文未找到一致的新发现来改变这一立场至今。然而,基于机器学习算法的包括基于局部、 "互相关/连接性 "和改进/标准化的图论标志的rsEEG测量的新技术,可能在未来增加定量脑电图的诊断效用,特别是在中低收入国家。
基于rsEEG测量对AD患者进行临床试验的分层
本文报告了ADD和ADMCI患者可能表现出一致的rsEEG测量变化。
最一致的发现是使用线性rsEEG测量,指向相对功率密度在头皮电极或源活动估计中的降低,以及在ADD和ADMCI患者中相对于年龄匹配的CU个体和由其他神经退行性和脑血管原因引起的认知缺陷匹配的患者中,后部区域占主导地位的alpha节律中降低的“互相关性”(例如,电极对之间的“谱相干性”和“相位滞后指数”或线性滞后源连接性)(表1)。此外,相同的线性rsEEG振幅测量和后部theta节律的“互相关性”反复与CU个体和AD患者出现显著认知衰退的概率较高相关(表2)。此外,往往报告δ频率下的rsEEG测量作为显著的标志物(表1和表2)。
建议使用这些线性rsEEG测量来对ADD和ADMCI患者进行分层,以便在临床试验中筛选患者的分层程序中使用。在第一步中,可以根据传统的NINCDS-ADRDA标准对可能的ADD和ADMCI患者进行选择,用于AD的临床诊断。在第二步中,这些患者可以接受标准的非侵入性和成本效益的rsEEG记录,并根据rsEEG测量中的异常程度(即基于中位数值的阈值)进行亚组分组。在第三步中,具有rsEEG测量最严重异常的ADD和ADMCI患者可以接受侵入性和相对昂贵的程序,提取CSF和神经影像学AD诊断生物标志物。只有对这些诊断生物标志物呈阳性的ADD和ADMCI患者才能参与观察性或干预性临床试验。这个程序将有助于节约财务资源,在招募阶段减少对CSF和神经影像学AD诊断生物标志物呈阴性的患者数量。此外,招募的那些rsEEG测量异常程度最高的患者可能是在ADD和ADMCI患者中测试新诊断程序和治疗干预的理想对象。
或者,如果上述临床试验旨在招募处于疾病早期的原发性AD患者,rsEEG记录可能有助于那些局部rsEEG测量正常或轻微异常的患者。
有关rsEEG测量在AD临床试验中的成本讨论,请参阅支持信息中《AD患者异常rsEEG测量的生理基础》。
AD的进展生物标志物在观察性和干预性AD临床试验中显然非常重要。在AD进展监测和治疗反应方面,最一致的发现是使用线性rsEEG测量得出的结果,指示在头皮电极或源活动估计中减少的功率密度以及在δ、θ、α和γ节律中减少的“相互关联性”(例如,“谱相关性”、“DTF”和电极对之间的“相位滞后指数”或线性滞后源连接)(表3)。
在这方面,这些rsEEG测量可以作为干预措施的次要终点,并且与提供更直接的进行性AD神经病理学和神经退行性测量的神经影像学生物标志物相比,具有补充价值。
总体而言,本文中审查的研究结果表明,需要国际共识倡议,以制定或完善多中心标准化的患者指导、rsEEG记录和选择无伪迹的rsEEG时段的操作规范,符合AD临床试验的标准。国际临床神经生理学联合会的一些倡议已经开始尝试这方面的工作。未来的双盲、前瞻性、多中心临床试验还可以比较不同的线性和非线性rsEEG测量(例如,“局部”、“相互关联性/连接性”和图论)在疾病监测、进展和干预方面的效果,以达成对最佳标准操作计算程序及其有效性和可靠性的共识。理想情况下,这些程序将基于经过良好建立的开放获取的互联网软件平台,以确保未来的可复制性(请参阅Colclough等人的研究中的两个有趣的示例191和Mahjoory等人的研究)。
我们还建议,应该尽一切努力使神经生理数据集(附带匿名化数据)成为开放获取。这种开放科学的方法不仅可以确保结果的可复制性,而且可以实现数据集的集成(允许大数据分析),并且可以加速该领域中算法/分类模型的开发/测试,推动数据科学的发展。为此,可以使用诸如OpenNEURO(https://openneuro.org/)之类的数据存储库。
在这些倡议中,监管机构(如食品药品监督管理局、欧洲药品管理局等)、国际临床神经生理学和神经病学科学协会以及阿尔茨海默病协会应扮演重要角色,因为预期验证过的rsEEG测量将作为生物标志物在临床试验中使用,与药物监管和许可相关。
本专家小组的建议总结在Box 3中。
Box 3:建议
“数据获取”在仔细的多中心标准化和协调的指导下进行,包括对患者和rsEEG记录的说明。 “数据分析”基于标准化选择无伪迹的rsEEG周期和通过开放访问的互联网软件平台提取线性的“局部”(例如,rsEEG功率谱密度)和“互相关/连接性”rsEEG测量,以确保可重复性。 “用于”AD患者的分层和疾病进展以及干预的监测。 “支持”跨部门的国际倡议,进一步验证rsEEG测量在AD中的应用。
6 结论
对于ADD和ADMCI患者的评估和疾病状态及进展的监测,rsEEG测量可以提供什么附加价值?
先前,IWG-2提出了两类用于评估ADD的生物标志物,即“诊断性”生物标志物(即测量疾病的病理生理特征,如脑淀粉样物质沉积以及脑脊液或PET技术直接测量总tau或磷酸-tau的标志物)和“进展或部位特异性”生物标志物(即测量具有特征性“AD特征”的区域特异性神经退行性进展,如FDG-PET和结构性MRI)。最近,NIA-AA研究框架提出了用于评估AD的三类生物标志物。他们将测量脑淀粉样物质沉积(即“A”生物标志物)和磷酸-tau(即“T”生物标志物)的CSF或PET技术称为“诊断性疾病”生物标志物。他们还将测量CSF中的总tau、FDG-PET代谢减退和脑萎缩的结构性MRI标志物称为“神经退行性/进展”生物标志物(即“N”生物标志物)。
在考虑到本文中所述rsEEG测量的“生理学”意义时,我们提出了“生理(P)生物标志物”的术语。按照这一观点,AD生物标志物框架可能变为“A”、“T”、“P”和“N”。这个“P”生物标志物(例如+或-)可能反映亚皮质和丘脑皮质环路以及升级激活系统的脆弱性或弹性,作为与AD状态和进展相关的额外和补充的重要信息。


